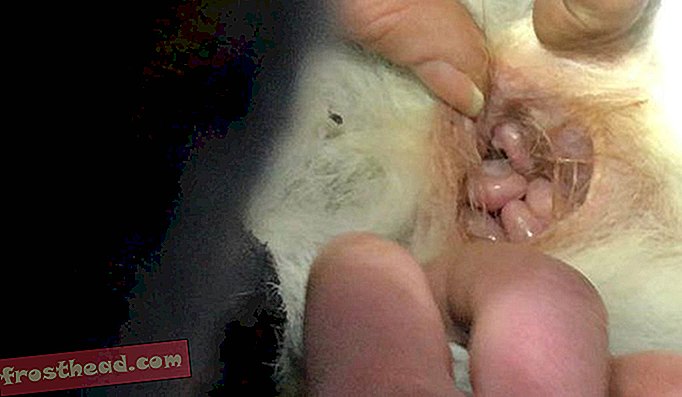
En bunion, måske har du ulykken at vide, er en benvækst, der dannes i bunden af din stortå. Når denne stød begynder at irritere resten af din fod, skal den gå.
Relateret indhold
- US Heroin overdoseringsfrekvens næsten firedobler
- Stater med medicinsk marihuana har færre smertestillende dødsfald
- Sort Mamba Venom slår Morfin som et smertestillende middel
At vinde ville være den rigtige reaktion her. I smerteskalaen kan en bunionektomi ikke sammenlignes med at have en savet lem; det er heller ikke særlig medicinsk risikabelt. Men da det "indebærer barbering af ekstra knogler og skæring af stortåen i halvdelen og fastgøring af den sammen igen, " siger David Soergel, medicinsk chef for lægemiddelfirmaet Trevena Inc, "det er faktisk en meget smertefuld operation." Det er værd at være værdig kvalitet gør det til den perfekte operation, hvor man kan teste banebrydende nye smertestillende midler - såsom Oliceridine, Trevenas nyeste og mest lovende opioidforbindelse.
I mere end 200 år har læger beroliget deres patients smerter med morfin, stoffet isoleret fra opiumsvalmuen og opkaldt efter Morpheus, den græske drømme gud. Og morfin har generelt levet op til sit ry som et effektivt smertestillende middel. Men på grund af hvordan det fungerer på det centrale nervesystem, har morfin også en række berygtede bivirkninger, fra kvalme til livstruende åndedrætsdepression til afhængighed. Så i 2014 var Soergel og hans team på jagt efter en sikrere - og mere effektiv - smertestillende middel. Håbet var, at Oliceridine kunne give ens eller bedre smertelindring end morfin, samtidig med at de grimme bivirkninger reduceres.
I forsøget modtog 330 bunionektomipatienter enten Oliceridin, morfin eller en placebo efter deres operation. De, der modtog begge lægemidler, rapporterede smertelindring inden for få minutter (i modsætning til timer for de fattige sjæle, der kun havde fået placebo). Men mens patienter, der fik 4 mg morfin rapporterede, at det tog omkring en halv time for dem at føle nogen lettelse, rapporterede de, der fik 4 mg Oliceridin, i gennemsnit kun to minutter. Oliceridin, som var designet til at drage fordel af forskernes nye forståelse af den underliggende neurovidenskab hos opioider, viste sig i sidste ende at være omkring tre gange så kraftig smertestillende som morfin. Endnu bedre, peer-reviewede studier viste, at det langt mindre sandsynligt ville forårsage farlige bivirkninger.
Resultatet "kunne være et betydeligt fremskridt inden for opioidfarmoterapi, " rapporterede Soergel og hans kolleger i tidsskriftet PAIN i juni samme år. De udvidede medikamentets potentiale i sammendraget af en anden undersøgelse, der blev præsenteret i oktober 2016 på det årlige møde i American Society of Anesthesiologists. "Denne nye handlingsmekanisme kunne føre til ... hurtig, effektiv analgesi med forbedret sikkerhed og tolerabilitet, " skrev teamet.
I dag er Oliceridine den eneste opioidforbindelse i sin art, der testes på mennesker. Det er nu i kliniske fase III-forsøg med resultater, der forventes i begyndelsen af 2017; hvis alt går godt, kunne det bringes på markedet inden for de næste par år, ifølge Trevena-medstifter Jonathan Violin. Lægemidlets potentiale er stort. Oliceridin - og andre forbindelser som det - kunne bare være den første af en række lægemidler med al den kraftige smertelindring af morfin, men langt færre ødelæggende bivirkninger. Og de er alle blevet muliggjort af vores nye forståelse af neurovidenskaben bag disse forbindelser. ”Dette kan være den første i det, du måtte tænke på som en ny klasse af opioider, ” siger Violin.
Og sandheden er, det handler om tid.
 En tablet med Vicodin, en af de mange receptpligtige opioider, der findes på markedet i dag. (Norma Jean Gargasz / Alamy)
En tablet med Vicodin, en af de mange receptpligtige opioider, der findes på markedet i dag. (Norma Jean Gargasz / Alamy) En revolution på vent
Der er få elementer af medicin, der ikke er kommet frem siden det 19. århundrede. I dag arbejder læger i antiseptiske operationsstuer og udøver antibiotika for at bekæmpe infektion snarere end knoglesave til fjernelse af gangrenøse lemmer. Moderne anæstesi er en sofistikeret medicinsk sammenvoksning sammenlignet med chloroform på en klud eller et skud med whisky. Men når det kommer til behandling af svær smerte, er vi stadig afhængige af det samme stof til stof, vi har brugt siden mindst 3400 fvt: opium.
Der er en grund til, at vi har været så loyale over for denne blomster: Den fungerer. Siden antikken har mennesker udnyttet kraften i opiumsvalmuen for at lette smerter, behandle sygdomme og generere eufori. Den sumeriske civilisation kendte valmuen som hul gil eller "glædeplante" for mere end 5.000 år siden; der er visuelle antydninger af valmuen i græske artefakter, der strækker sig tilbage til 1500 f.Kr. romerske læger i det første og andet århundrede anbefalede opium blandet med vin inden amputationen af lemmer. I 1784 registrerede den britiske kirurg James Moore den første kendte brug af opium for at lette smerter efter operationen.
I 1805 ændrede den tyske farmaceut Friedrich Serturner spillet ved at isolere morfin fra opium. En anden udvikling i det århundrede ville udvide den succes og forbedre levering og destillation af denne potente forbindelse. I 1850'erne gav udviklingen af den hypodermiske injektionssprøjte mulighed for, at nøjagtige doser af morfin kunne leveres direkte i en patients blodbane, hvilket ville være nøglen til amputationer af felthospitaler under den amerikanske borgerkrig. I 1890'erne blev morfin udvidet til en række morfinlignende medikamenter kendt samlet som opioider.
Sammenlagt har denne pakke medikamenter - som i dag fås som piller, injektioner, slikkepinde og plaster - revolutioneret behandlingen af smerter. Men lettelsen, de bringer, er ikke uden omkostninger. Morfin skulle også vise sig at have en mørk side. Selv i det 19. århundrede var afhængighed blandt soldater efter sigende udbredt nok til at tjene monikeren "soldatens sygdom."
I dag er morfinafhængighed Amerikas sygdom. I USA har overskrivning og misbrug af opioid medicin ført til en voksende afhængighedskrise. Siden 1999 er antallet af dødelige opioid overdoser i USA firedoblet. Så har antallet af recept, der er skrevet til opioidsmertemedicin. Ifølge Debra Houry, direktør for National Center for Injury Prevention and Control at CDC, blev 249 millioner opioidrecepter skrevet i 2013 - nok til, at enhver amerikansk voksen havde deres egen flaske. Og mange, der bliver afhængige af disse medicin, går videre til et billigere og farligere stof på sortmarkedet: heroin.
I 1890'erne begyndte Bayer-lægemidler at markedsføre heroin - hvilket er fremstillet ved at anvende den kemiske proces med acetylering på morfin - som et angiveligt mere potent og mindre vanedannende alternativ til morfin. Heroin ville vise sig at være omkring to til fire gange mere potent end morfin, men hævder, at det var mindre vanedannende, ville vise sig ubegrundet på dramatisk vis. I 2015 anslåede American Society of Addiction Medicine næsten 600.000 amerikanere at være afhængige af heroin. Ifølge kirurggeneralens rapport om afhængighed, der blev frigivet i november, døde mere end 28.000 amerikanere af brugen af receptpligtige opioider eller heroin i 2014.
Hvad kan der gøres ved denne epidemi af meget vanedannende, ofte dødelige smertestillende? Det åbenlyse svar, du måske tror, ville være at grøfte opioider. Problemet er, at der kun er så meget smerte, som en patient kan forventes at have, og indtil videre har kun opioider været tilgængelige for at lindre den.
Men det kan være ved at ændre sig. Ny forskning i de underliggende molekylære mekanismer for opioider har gjort det muligt at opdage nye forbindelser, der muligvis bare muliggør lindring af smerter uden nogle af de værste bivirkninger af traditionelle opioider. (Videnskabsforfatter Bethany Brookshire skrev for nylig om nogle af disse nye forbindelser til Science News .) Hvis denne forskning bærer frugt, kan morfin snart gå vejen for knoglesag fra det 19. århundrede - hvilket gør plads til en revolution af nye medikamenter, der ikke forårsager fysisk afhængighed, og som det er umuligt at overdosis på. Medikamenter, som risikoen for afhængighed er ubetydelig eller endda forsvinder helt.
Hvis de panorerer.
 Laura Bohn i sit laboratorium på Scripps Research Institute. (Jeremy Pyle / TSRI Outreach)
Laura Bohn i sit laboratorium på Scripps Research Institute. (Jeremy Pyle / TSRI Outreach) Den dobbelte dør
Traditionelle opioider - inklusive morfin, den potente syntetiske fentanyl og Vicodin, du får fra din tandlæge - fungerer alle ved at binde til opioidreceptorer i nervesystemet. Disse receptorer findes i tre varianter: mu, delta og kappa. Det er ved mu-opioidreceptoren, at opioider fungerer deres magi og aktiverer en kaskade af cellulær signalering, der udløser deres smertelindrende virkning. På sprog neurovidenskab er opioider mu-receptor “agonister” i modsætning til “antagonister”, som er forbindelser, der binder til en receptor og blokerer for at forhindre cellulær signalering. Når en opioid binder til mu-opioidreceptoren, nedsætter den i sidste ende lydstyrken på nerverne, der kommunikerer smerte. Dette er selvfølgelig den ønskede effekt.
Desværre er det ikke alt, hvad det gør. Opioider frigiver også neurotransmitteren dopamin, hvilket forårsager eufori og kan føre til afhængighed. Disse forbindelser hæmmer også nerveceller fra at affyres mere generelt, herunder i dele af hjernen, der regulerer vejrtrækning - hvilket kan være farligt. Tag for meget af en opioid, og du holder op med at trække vejret og dø; det er, hvad det er at overdosere. CDC vurderer, at 91 amerikanere dør hver dag af en opioid overdosering. Bivirkningerne fortsætter fra forstoppelse til kvalme til den hurtige udvikling af tolerance, så der er behov for stadig højere doser til den samme effekt.
I lang tid troede man, at dette kun var pakkeaftalen. For at opnå lindring af smerter, var du nødt til at leve med bivirkningerne, da de var resultatet af mu-opioidreceptorsignalering. Så kom Laura Bohn, der satte scenen for en ny videnskab om smertelindring.
I 1999 var Bohn en postdoktoral forsker i Marc Caron-lab ved Duke University, hvor han studerede, hvordan opioidreceptoren fungerede i mus. Dette var grundlæggende forskning på det tidspunkt - det vil sige, det blev ikke gennemført som en del af en plan for at udvikle nye smertestillende medicin. Snarere, siger hun, var det den slags videnskab for videnskabens skyld, der får øje på budgetnedskæringer. ”Du kan huske fra 1980'erne, at alle politikere ville sige, 'Sæt en mus på en varm plade, hvordan kan det hjælpe?'” Siger Bohn, der nu er farmakolog ved Scripps Research Institute i Jupiter, Florida. ”Det er sådan, det hjælper.”
På det tidspunkt vidste forskerne, at der var to proteiner involveret i opioidreceptorsignalering: G-proteinet, og et andet kaldet beta-arrestin. For at undersøge funktionen af beta-arrestin tog Bohn en gruppe af beta-arrestin “knockout” mus - dyr, der var blevet genetisk manipuleret, så deres kroppe ikke indeholdt beta-arrestin - og gav dem morfin sammen med en kontrolgruppe af regelmæssige mus. Det var velkendt, hvordan mus reagerede på morfin, så enhver anden reaktion i knockout-musene ville give ledetråde til rollen som beta-arrestin.
Når du giver dem morfin, plejer normale mus at løbe rundt i tilsyneladende glæde. Knockout mus gjorde det ikke. ”Da vi begyndte at behandle dyrene med morfin, var det bare virkelig åbenlyst forskellen mellem de vilde typer og dem, der manglede beta-arrestin, ” siger Bohn. ”Åbenbart til det punkt, hvor et seks år gammelt barn gik ind i laboratoriet og sagde: 'Disse mus er forskellige fra de andre mus.'” Senere forskning viste endnu mere lovende tegn: knockout-musene viste mindre forstoppelse og respirationsdepression, når givet morfin, og morfin viste sig at være mere potent til at lindre smerter.
Pludselig så det ud til, at den dobbeltkantede hypotese ikke nødvendigvis var sand. Virkningen af opioider, syntes det, behøvede ikke at være en pakkeløsning - du kunne slå nogle af de ønskede effekter ud og forlade andre. Som Trevenas Violin udtrykker det: "I mangel af beta-arrestin var morfin et bedre lægemiddel."
Den vigtigste opdagelse var, at opioid “receptorer ikke er tænd / sluk-switches, ” forklarer Bohn. ”Det er ikke 'lås og nøgle', hvor nøglen går ind og drejer låsen, og den bare åbner.” I stedet er receptoren som en dobbelt haveport, der kan åbnes på to veje, G-protein og beta-arrestin stier. Brug morfin til at låse porten op, og den svinger åbent som en enhed på begge stier. Skift selve porten, så beta-arrestinsiden forblev låst - som i Bohns knockout-mus - og du kunne åbne for bare G-proteinstien og høste de afgørende fordele ved morfin med færre bivirkninger.
Det siger Bohn ikke altid, siger Bohn, at bivirkninger og ønskede effekter opdeles pænt i beta-arrestin og G-protein-signalering på hver receptor. Men "dette er ting, vi er nødt til at lære, " siger hun, "det ringer os tilbage til grundlæggende forskning og virkelig forståelse af fysiologien."
Problemet er, at du ikke kan ændre mu-receptorporten i mennesker; det ville kræve genetisk manipulation før fødslen. Det, der var behov for, var derfor et andet sæt nøgler: Nye medikamenter, G-protein "partisk-agonister", som kun ville åbne G-proteinsiden af porten og efterlade Pandoras æske med skadelige bivirkninger sikkert låst. I 2004 begyndte Bohn at lede efter disse nøgler; hun blev sammenføjet i 2008 af folkene på Trevena. ”De tog dette mod en lægemiddeludviklingssti, og jeg tog det mod en akademisk vej, ” siger Bohn. ”Jeg tror, vi alle slags kommer rundt og ser, at ja, der er noget løfte om dette.”
 En vildledende reklame for Vicodin, offentliggjort i 1992. (North Carolina Medical Journal, bind 53)
En vildledende reklame for Vicodin, offentliggjort i 1992. (North Carolina Medical Journal, bind 53) The New Morphine (s)
Med hensyn til at komme på markedet og i patienters recept, springer Oliceridine i øjeblikket foran sine konkurrenter. Men det er ikke det eneste stof, der viser løfte. En anden forbindelse, kendt som PZM21, ser ud til at nedtrykke åndedræt - hvilket betyder at langsomt eller hindre vejrtrækning - i mindre grad end endda Oliceridin i gnavere, ifølge arbejde offentliggjort i tidsskriftet Nature i september. Der er også indikationer på, at det kunne være mindre givende, dvs. mindre vanedannende end traditionelle opioider.
Ligesom Oliceridine er PZM21 en opiaidforbindelse med en partisk-agonist, men den har en anden kemisk struktur. Forskere er stadig uklare, hvad med den forskel i struktur, der tegner sig for de forskellige virkninger af de to forbindelser, ifølge farmakolog Brian Shoichet fra University of California i San Francisco, en af forfatterne af Nature- undersøgelsen. "Bortset fra klinisk brug er PZM21, [Oliceridine] og andre værktøjsmolekyler, der kan hjælpe os med at forstå afhængighedsbiologien, " siger han. ”Sammen med den rigtige farmakologi kunne det virkelig udvide vores muligheder for at opdage meget nye molekyler, der giver meget nye biologiske effekter.”
Andre undersøgelseslinjer går ud over Bohns partiske-agonistiske tilgang. På University of Maryland School of Pharmacy har forsker Andrew Coop brugt mere end et årti på at arbejde på et syntetisk opioid kaldet UMB425, idet den har nøjagtigt den modsatte tilgang fra forskere, der arbejder med partiske agonister som Oliceridine og PZM21. I stedet for at designe et stof, der er mere og mere selektivt for at ramme en bestemt sti, spørger han, ”hvad med hvad med at gå den anden vej og ramme et andet mål, der modulerer det?” Denne tilgang - ved at bruge et stof til at ramme flere receptorer - er kendt som polyfarmakologi. Resultatet er et lægemiddel, der i det mindste i gnavere lindrer smerter bedre end morfin med mindre udvikling af tolerance.
Og det er bare spidsen for smertestillende revolution. Et andet eksempel på den polyfarmakologiske tilgang er Stephen Husbands arbejde, en medicinsk kemiker ved Bath University. Hans forbindelse, BU08028, ligner strukturelt det med buprenorfin, et lægemiddel, der bruges til at behandle opioidforstyrrelser. Det virker både på mu-opioidreceptoren og nociceptinreceptoren, som er relateret til opioidreceptorerne. Hos aber viste ægtemænd BU08028 lindrer smerter uden at forårsage afhængighed, afhængighed eller depression af vejrtrækning.
Nye smertestillende medicin kunne kun være begyndelsen. Mange receptorer i hjernen - inklusive dopamin-, serotonin- og cannabinoidreceptorer - kan også målrettes ved hjælp af den partiske-agonistiske tilgang, hvilket muligvis giver bedre antidepressiva eller andre lægemidler. Trevena studerer allerede en forbindelse, der fungerer som en partisk-agonist ved delta-opioidreceptoren som en mulig migrænehovedpine-medicin, ifølge Violin. Tidligere lægemidler, der målrettede delta-receptoren, forårsagede anfald, men Trevenas forbindelse gør det ikke (teorien er, at anfaldene blev forårsaget af beta-arrestin-signalering).
Coop, der håber at teste UMB425 i primater og en dag hos mennesker, siger alt, at konkurrence er en god ting. ”Det er godt at have alle disse forskellige mekanismer fremad, ” siger han. ”Det øger vores chancer for, at en af disse faktisk kan klare det.”
En dosis af forsigtighed
Potentialet for disse næste generations opioider er stort. Men inden for lægemiddeludvikling er intet garanteret. Oliceridin kan ramme et uforudset problem i kliniske forsøg; UMB425 kunne vise sig at være vanedannende eller for giftig hos mennesker. En kemiker fra det sorte marked kunne syntetisere en af disse nye forbindelser og forårsage et lovmæssigt tilbageslag. (Det er ingen abstrakt bekymring: Sidste år annoncerede DEA midlertidigt sin hensigt om at placere de aktive komponenter i Kratom-anlægget i det restriktive tidsplan I efter rapporter om personer, der bruger anlægget til at behandle smerte eller opioidafhængighed. Det kan hindre forskning i mitragynin pseudoindoxyl, en anden lovende ny opioid baseret på forbindelser fundet i Kratom.)
Givet nogle tvivlsomme industriløfter om afhængighed og smertestillende medicin i fortiden, er Bohn især opmærksom på at hævde for meget, for tidligt. ”Jeg er meget konservativ med hensyn til dette, fordi jeg synes, vi skal være meget omhyggelige med ikke at gentage fortidens problemer og oversætte en opiat og sige, at det ikke vil være vanedannende - som visse virksomheder gjorde, ” siger hun. Hendes filosofi fremover er at antage, at alle disse stoffer vil have en vis risiko for afhængighed og at behandle dem med forsigtighed. På samme tid, selvom afhængighed forbliver en fare, vil medikamenter, der eliminerer andre bivirkninger, stadig repræsentere et stort skridt fremad.
Alligevel rejser Bohns tilgang et afgørende spørgsmål: Kan afhængighed nogensinde afhjælpes fuldt ud - eller vil smertestillende medicin altid have en risiko for mørke konsekvenser? Afkobling af de to synes bestemt videnskabeligt muligt, siger Coop, i betragtning af de nuværende modeller af partisk-agonisme og polyfarmakologi. Men afhængighed er et mangesidet udyr, og der kan altid være nye komponenter, der endnu ikke er forstået. Der er muligvis ingen magisk kugle, indrømmer Coop. "Der har været flere falske daggry med hensyn til at adskille den ønskede fra de uønskede effekter af opioider, " siger han, "og de nuværende fremgangsmåder kan måske ikke igen oversætte til behandling af mennesker i klinikken."
En lille spænding er med andre ord berettiget, men send ikke morfin til hallen med medicinske nysgerrigheder lige endnu. ”Jeg synes, vi skal gå forsigtigt, men også realisere den enorme mulighed, ” siger Bohn. ”Dette er en reel mulighed inden for farmaceutisk udvikling.”
Redaktørens note 16. januar 2017: På grund af en redigeringsfejl angav billedtekst oprindeligt, at Vicodin-annoncen, der blev vist i North Carolina Medical Journal, blev offentliggjort i 1940. Tidsskriftet begyndte faktisk i det år.