Zebrafisk er kun nogle få centimeter lang, men de har nogle store størrelser. Når deres hjerter eller hjerner er beskadiget, regenererer de sig. Når deres finner er afskåret, vokser de tilbage. Når de er blinde, kan de genvinde evnen til at se.
Det er denne sidste evne, der er genstand for nogle potentielt banebrydende ny forskning. Vanderbilt-videnskabsmænd har måske opdaget nøglen til regenerering af zebrafisk nethinde. Hvis processen kan replikeres hos mennesker, står den i kraft til nye behandlinger for blindhed forårsaget af nethindesygdom og skade.
”Da jeg lærte mere og mere om, hvordan zebrafisk er i stand til at regenerere de fleste væv og organer, blev jeg fascineret, især med det faktum, at zebrafisk nethinden kan blive beskadiget for at forårsage blindhed, men det tager kun ca. tre til fire uger, før synet er genoprettet, ”Siger James Patton, professor i biologisk videnskab ved Vanderbilt, der ledede forskningen.
Zebrafisk, en ferskvandsmand opkaldt efter deres karakteristiske striber, har længe været et populært testemne for forskere. De avler let i fangenskab, vokser hurtigt, og da babyer er helt gennemsigtige, hvilket gør det nemt at studere deres organer. Så er der deres regenererende evner. Da de deler 70 procent af menneskers genetiske kode, er det ofte muligt at bruge dem til at studere menneskets genetiske træk og sygdomme.
Strukturen og celletyperne af zebrafisk nethinder er næsten identiske med mennesker. Hver indeholder tre lag nerveceller: lysdetekterende fotoreseptorer, signalintegrerende vandrette celler og ganglionceller, der videregiver visuel information til hjernen.
”Så jeg blev endnu mere fascineret af, hvorfor mennesker ikke kan regenerere beskadigede nethinder og fiskekande, ” siger Patton.
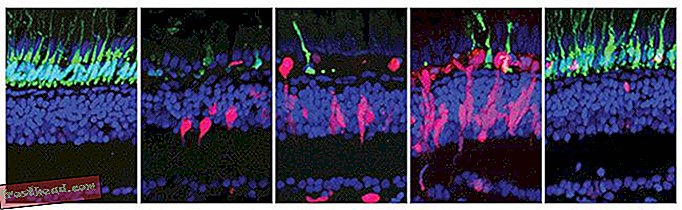 Disse fem billeder, der spænder over 28 dage, viser, hvordan regenerering sker i nethindens zebrafisk. Stænger er vist i grønt, regenererende celler vises i rødt, og alle andre celler er blå. Regenererende celler erstatter de døende stænger. (The Patton Lab / Vanderbilt)
Disse fem billeder, der spænder over 28 dage, viser, hvordan regenerering sker i nethindens zebrafisk. Stænger er vist i grønt, regenererende celler vises i rødt, og alle andre celler er blå. Regenererende celler erstatter de døende stænger. (The Patton Lab / Vanderbilt) Nethindeskade ligger bag mange af de førende årsager til blindhed i den udviklede verden. Disse årsager inkluderer makuladegeneration, en ofte aldersrelateret sygdom, hvor en del af nethinden bliver beskadiget, hvilket forårsager sløret og blanke pletter i synet; diabetisk retinopati, hvor diabetes skader blodkar i nethinden; og retinitis pigmentosa, en genetisk tilstand, der forårsager degeneration af nethindens stavfotoreceptorceller. Da humane nethinder ikke regenererer, er enhver retinal skade forårsaget af sygdom eller skade permanent.
Patton og hans team blev nysgerrige efter, hvordan nøjagtigt regenerering af zebrafisk nethinden indledes. Tidligere undersøgelser har antydet, at vækstfaktorer, der udskilles af farvende fotoreceptorer i fiskernes øjne, muligvis kan starte processen, idet de stammer celler i øjnene for at begynde at differentiere sig (går tilbage til et tidligere udviklingsstadium) og derefter differentieres til nye nethindeceller. Men Mahesh Rao, en af Pattons kandidatstuderende, fik ideen til at se på neurotransmitteren GABA, en kemisk messenger i hjernen, der reducerer aktiviteten af neuroner, og bemærkede, at GABA var fundet at kontrollere stamcelleaktivitet i muses hjerner.
Holdet testede Rao's idé ved at blende zebrafisk - dette kan gøres ved at sætte dem i mørke i et par dage og derefter udsætte dem for skarpt lys - derefter give dem GABA-stimulerende stoffer. De gav også GABA-sænkende medikamenter til normalt seende zebrafisk. De fandt, at de blinde fisk, der fik GABA-stimulerende medikamenter, ikke kunne regenerere deres nethinder normalt, mens de normale fisk med sænkede GABA-niveauer begyndte at regenerere deres nethinder. Dette antydede, at det faktisk var en sænket koncentration af GABA, der startede retina-regenereringsprocessen.
Resultaterne blev offentliggjort denne måned i tidsskriftet Stem Cell Reports .
 L til R: James Patton, Mahesh Rao og Dominic Didiano i zebrafisklaboratoriet (The Patton Lab / Vanderbilt)
L til R: James Patton, Mahesh Rao og Dominic Didiano i zebrafisklaboratoriet (The Patton Lab / Vanderbilt) ”Vi håber at bruge fiskemodellen til at forstå de faktorer og mekanismer, der regulerer retina-regenerering i håb om, at vi kan anvende erfaringer til mennesker, ” siger Patton.
Holdet begynder at teste GABA-teorien om mus. Hvis det fungerer, vil det være på menneskelige forsøg, der tester, om GABA-hæmmere kan stimulere regenerering af nethinden.
Hvis forskningen virkelig viser sig vellykket hos mennesker, kan nogle af de næsten 40 millioner blinde mennesker verden over en dag have en lille, stribet fisk at takke for.