Den sidste mandlige, hvide, hvide næsehorn - han hed Sudan - døde i marts og efterlod kun to medlemmer af underarten: hans datter og barnebarn.
Tidligere ville disse skarpe fakta have stavet slutningen. Men forskere ved San Diego Zoo's Institute for Conservation Research - hjemsted for et frostigt menagerie, kaldet Frozen Zoo - arbejder for at give nordlige hvide næsehorn en anden chance. Siden 1975 har instituttet indsamlet væv fra væsener, nogle truet og nogle ikke, for derefter at dyrke cellerne i laboratoriet og bevare dem på en kølig 321 grader under nul Fahrenheit.
Zoologiske haver bruger allerede reproduktionsteknologier såsom in vitro-befrugtning til dyr som gorillaer og kunstig befrugtning til pandaer. (Andre steder overvejer forskere fordelene ved at genoplive uddøde arter som den uldne mammut og passagerduen, skønt de skulle bruge gammelt DNA til det.) Frozen Zoo har brugt dets bevarede sæd til at skabe fasanerunger, og er gået så langt som at lave embryoner af geparder og befrugte æg fra sydlige hvide næsehorn.
Nu håber dens dyreholdere, at deres dusin nordlige hvide næsehornsprøver bliver forældre til en ny generation på en anden måde: ved hjælp af stamcelle-teknologi til at omdanne det bevarede hvide næsehorn hudvæv til æg og sæd.
Instituttets forskning går ud over babyfremstilling. Forskere der arbejder på metoder til genetisk identifikation af kød fra primater og duikerantiloper, der er blevet jagtet ulovligt. Og i fremtiden bruger de muligvis dens samling til at gendanne genetisk mangfoldighed til truede sortfodede ildere.
Udvidelse af sådanne bestræbelser vil kræve et globalt netværk af frosne zoologiske haver, skriver Oliver Ryder, instituttets direktør for bevaringsgenetik, og medforfatter Manabu Onuma i den årlige gennemgang af dyrebiosciences .
Ryder, der har været på instituttet, siden det startede, talte med Vidende om Frozen Zoo's fortid, nutid og fremtid. Denne samtale er redigeret for længde og klarhed.
Hvordan begyndte Frozen Zoo?
Vi vil gerne sige, at Frozen Zoo startede, da Dr. Kurt Benirschke kom til San Diego Zoo i 1975. Dr. Benirschke, der døde i 2018, var interesseret i fertilitet og kromosomer. Teknologien til at fryse celler og optø dem med gendannet funktion var stadig temmelig ny - den blev først udført med sædceller i 1949 - men det åbnede for alle mulige muligheder. At have cellekulturer til at fryse, genoplive og dyrke flere celler fra, se på kromosomer, var et virkelig betydningsfuldt fremskridt. Andre forskere gjorde dette, men mest inden for humanmedicinsk forskning.
Dr. Benirschke var især interesseret i at beskrive kromosomer fra forskellige arter. Vi benyttede enhver lejlighed, der kom op for at samle en ny art. Der var en tillid til, at celler, der blev banket, ville finde anvendelser langt ud over, hvad der kunne tænkes på det tidspunkt.
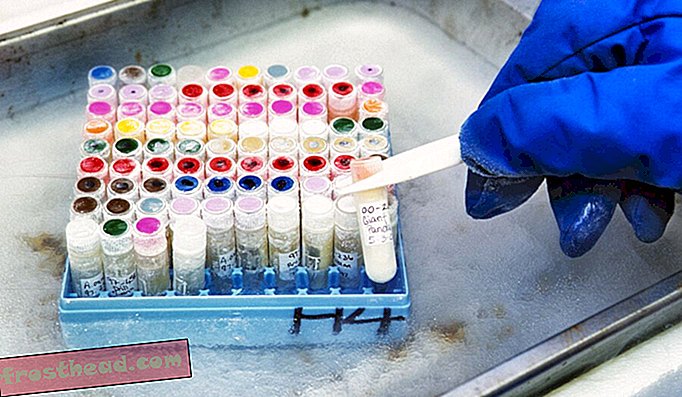 I den frosne zoologiske have er hætteglas som disse "dyrehylstre." Hver indeholder sædceller eller celler, der er dyrket af en smule dyrehud eller andet væv. De opbevares i flydende nitrogen ved -321 grader Fahrenheit og optøes, når forskere vil bruge dem. (San Diego Zoo Global)
I den frosne zoologiske have er hætteglas som disse "dyrehylstre." Hver indeholder sædceller eller celler, der er dyrket af en smule dyrehud eller andet væv. De opbevares i flydende nitrogen ved -321 grader Fahrenheit og optøes, når forskere vil bruge dem. (San Diego Zoo Global) Du sluttede dig også til Frozen Zoo, derefter kaldet Center for Reproduktion af truede arter, i 1975. Kan du huske det første dyr, du nogensinde har konserveret celler fra?
Det var en kinesisk muntjac, et bjælkende rådyr. Der var en der havde et brud og blev repareret af ortopædkirurger. De måtte fange det og bedøve det for at skifte rollebesætningen, så jeg var i stand til at komme og lave en hudbiopsi.
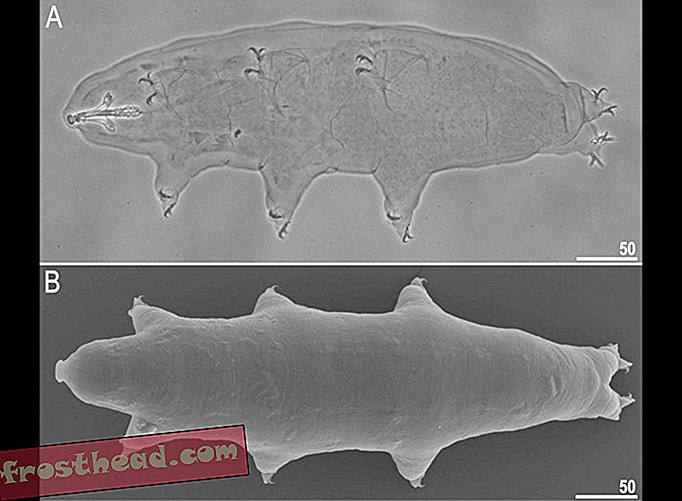
Den bjælkende hjort er interessant. Der er både kinesiske og indiske muntjacs, og den gennemsnitlige person vil blive udfordret til at identificere meget forskel mellem de to. Selvom den kinesiske muntjac har 46 kromosomer, har den indiske muntjac det laveste kendte kromosomantal hos pattedyr: seks hos kvinder, syv hos mænd.
De af os, der var interesseret i evolution, i hvordan kromosomer udviklede sig og hvordan arter dannes, blev udfordret af denne "skandale", som den blev kaldt. Vi ved nu, at kromosomerne smeltede sammen i forfæderen til den indiske muntjac. Hvad der udløste denne fusion vides ikke, men det skal have fundet sted. En hybrid mellem de to blev lavet i Kina; det havde tre store kromosomer og 23 små. Den levede, men den kunne ikke gengive sig.
En anden gang, i 1980, husker jeg, at patologen sagde til mig, ”Vi har et rigtig interessant og sjældent dyr i nekropsirommet. Du skulle få en prøve. ”Og det var en nordlig hvid næsehorn. Denne prøve leverede materialet år senere til at udføre den første genetikundersøgelse, hvor man sammenlignede nordlige og sydlige hvide næsehorn.
Gå nu hurtigt frem til nutiden, og vi har et ambitiøst genetisk redningsprojekt for at forhindre udryddelse af de nordlige hvide næsehorn, og det afhænger af de 12 nordlige hvide næsehornskulturer, som vi har banket gennem årene.
Hvordan kan du bruge disse celler til at redde den nordlige hvide næsehorn?
Fra de bankede hudprøver har vi frosne celler, der kaldes fibroblaster. Vi tiner disse kulturer og forvandler dem til det, der kaldes inducerede pluripotente stamceller. Disse kan teoretisk set forvandle sig til næsten enhver form for celle i kroppen: De kan fremstille bankende hjerteceller, de kan fremstille nerveceller.
Vores eventuelle mål er at omdanne stamceller til æg og sæd, så vi kan lave embryoner. Med andre ord vil disse fibroblaster kunne få babyer.
Dette er gjort i labmus, men endnu ingen andre arter. Indtil videre har vi induceret pluripotente stamceller fra nordlige hvide næsehorn. Nu finjusterer vi metoder til at bekræfte, at de er pluripotente. Der er et andet hold, der arbejder med en besætning af kvindelige sydlige hvide næsehorn, som vi planlægger at bruge som surrogater. Vi er mindst et årti væk fra en baby, hvid næsehorn, men vi gør fremskridt.
Hvis du ville have spurgt mig i 1985, kan du tage en celle fra Frozen Zoo og forvandle den til et dyr, ville jeg have sagt nej. Nu planlægger vi at gøre det i laboratoriet her.
 Friske oocytter (æg) samlet fra en sydlig hvid næsehorn. For at hjælpe med at bringe den nordlige hvide næsehorn fra randen af udryddelse, håber Frozen Zoo-forskere at omdanne de bevarede nordlige hvide næsehornshudceller til æg og sæd og implantatembryoer til en sydlig hvid næsehorn. (TB Hildebrandt et al. / Nature Communications 2018)
Friske oocytter (æg) samlet fra en sydlig hvid næsehorn. For at hjælpe med at bringe den nordlige hvide næsehorn fra randen af udryddelse, håber Frozen Zoo-forskere at omdanne de bevarede nordlige hvide næsehornshudceller til æg og sæd og implantatembryoer til en sydlig hvid næsehorn. (TB Hildebrandt et al. / Nature Communications 2018) Hvad laver du andet med prøver fra Frozen Zoo?
Vi er en fremragende kilde til genomprojekter. Vi har bidraget med prøver til noget som 140 helgenom-sekventeringsprojekter.
Vi samarbejder med Broad Institute i Cambridge, Massachusetts, om 200 pattedyrsprojekt, som vil sammenligne humant DNA med 199 andre pattedyr. Det vil hjælpe forskerne med at forstå, hvilket kernesæt der er så vigtigt, at de er blevet bevaret i os og andre dyr. Og jeg er involveret i Vertebrate Genomes Project for at rækkefølge alle 66.000 levende hvirveldyrarter. Disse genomer afslører mange interessante ting om en dyrepopulation, dens migrationsmønstre og om den er hybridiseret med andre arter. Denne type genetisk analyse åbner et forbløffende nyt vindue om, hvordan livet fungerer.
I din gennemgang drøftede du oprettelsen af en global biobank for vilde dyr. Hvorfor er det vigtigt?
Selvom San Diego Zoo har sin frosne zoologiske have, med mere end 1.000 arter, er det en lille brøkdel af verdens biodiversitet. Der er omkring 26.500 truede arter, der er blevet navngivet - og mere, der ikke er anført på listen.
Næste år vil der være mindre biodiversitet end der er nu. Så vi burde være bank, mens vi kan. Det skal gøres i forskellige lande, så de har deres egne genetiske ressourcer banket.
Du sagde, at da du ankom Frozen Zoo for 44 år siden, kunne du ikke have forestillet dig at dyrke hele dyr fra celler. Hvilket projekt ville du elske at se, at Frozen Zoo varetager i de næste 44 år?
Når artsbestanden krymper, mister de også værdifulde versioner af gener, der kun var til stede i visse dyr. Genpuljen bliver en genpyt. Jeg kan forestille mig, at vi ved hjælp af bankmateriale i fremtiden kunne gendanne genetisk variation.
Hvordan ville du gøre det?
Vi bliver nødt til at forvandle celler til dyr. For eksempel kan du tage et kvindedyr, der bor i naturen, og overføre et embryo med nogle nyttige gener til hende.
Nogle vil måske sige, at at bringe mistede gener eller næsten uddøde arter tilbage spiller Gud.
Men mennesker har gjort det i lang tid: Vi har forårsaget arter udryddelse. Vi har uændret ændret deres levesteder. Vi har ændret deres opførsel. Vi har blandet dem. Vi har ændret deres miljøer, deres rovdyr, deres sygdomme. Alle disse ting har vi allerede gjort.
Brug af bankede prøver til at fremme mangfoldighed ville give os en chance for at ændre den naturlige verden på en positiv måde.
 Knowable Magazine er en uafhængig journalistisk indsats fra årlige anmeldelser.
Knowable Magazine er en uafhængig journalistisk indsats fra årlige anmeldelser.